Оксиды азота (закись, ангидриды, диоксид): свойства и формулы веществ
Содержание:
- Фармакология
- Свойства
- Естественное разложение NO x
- Признаки употребления
- Оксид азота: свойства и все характеристики
- Функция ЕСЛИ в Excel
- Сферы применения
- Углекислый газ и мы: чем опасен СO2
- Физические свойства оксида азота (IV):
- Химические свойства
- релиз
- Использует [ редактировать ]
- Оксид углерода CO2(IV) — углекислый газ
Фармакология
Добавочный оксид азота
NO, который синтезируется в организме и впоследствии высвобождается в кровь, имеет период полувыведения в 5 секунд или меньше, при этом в лабораторных условиях могут создаваться некоторые комплексы для увеличения периода полувыведения до 445 с или около того в целях исследования. Эти короткие периоды полувыведения свидетельствуют о быстром распаде молекулы оксида азота на составляющие (азот и кислород), при этом надлежащее хранение NO может увеличивать срок хранения, как было подтверждено, только до 5 дней, при использовании майларовых баллонов, которые замедляют разрушение. В связи с низкой устойчивостью вне организма, оксид азота по существу никогда не используется в качестве добавки, скорее используются соединения, которые могут сохраняться в крови на протяжении времени, достаточного для непрерывной выработки нового NO.
Оксид азота по существу неустойчив и имеет короткий период полувыведения; он оказывает полезное действие немедленно, но не имеет значения в качестве добавки и сам по себе. Добавка NO требует других соединений, которые оказывают влияние на внутреннюю систему выработки оксида азота.
Свойства
Физические
Плотность при нормальных условиях 1,98 г/л. При атмосферном давлении диоксид углерода не существует в жидком состоянии, переходя непосредственно из твёрдого состояния в газообразное. Твёрдый диоксид углерода называют сухим льдом. При повышенном давлении и обычных температурах углекислый газ переходит в жидкость, что используется для его хранения.
Углекислый газ легко пропускает ультрафиолетовые лучи и лучи видимой части спектра, которые поступают на Землю от Солнца и обогревают её. В то же время он поглощает испускаемые Землёй инфракрасные лучи и является одним из парниковых газов, вследствие чего принимает участие в процессе глобального потепления. Постоянный рост уровня содержания этого газа в атмосфере наблюдается с начала индустриальной эпохи.
Химические
По химическим свойствам диоксид углерода относится к кислотным оксидам. При растворении в воде образует угольную кислоту. Реагирует со щёлочами с образованием карбонатов и гидрокарбонатов. Вступает в реакции электрофильного замещения (например, с фенолом — реакция Кольбе) и нуклеофильного присоединения (например, с магнийорганическими соединениями).
Биологические
Диоксид углерода играет одну из главных ролей в живой природе, участвуя во многих процессах метаболизма живой клетки. Диоксид углерода получается в результате множества окислительных реакций у животных, и выделяется в атмосферу с дыханием. Углекислый газ атмосферы — основной источник углерода для растений. Однако, ошибкой будет утверждение, что животные только выделяют углекислый газ, а растения — только поглощают его. Растения поглощают углекислый газ в процессе фотосинтеза, а без освещения они тоже его выделяют.
Диоксид углерода не токсичен, но не поддерживает дыхание. Большая концентрация в воздухе вызывает удушье (см. Гиперкапния). Недостаток углекислого газа тоже опасен (см. Гипокапния)
Углекислый газ в организмах животных имеет и физиологическое значение, например, участвует в регуляции сосудистого тонуса (см. Артериолы).
Естественное разложение NO x
Процессы образования и разрушения оксидов азота в атмосфере чрезвычайно сложны. Они состоят из множества реакций, на которые в той или иной степени влияют преобладающая температура, сила солнечного света, давление, загрязнение и соответствующие соотношения концентраций. Когда молекулы поднимаются в атмосферу, например, с одной стороны, вероятность реакции уменьшается из-за уменьшения давления, с другой стороны, некоторые столкновения с инертными молекулами устраняются, и интенсивность излучения увеличивается. Вот почему период полураспада веществ, участвующих в реакциях, меняется с высотой, а некоторые промежуточные продукты, которые очень недолговечны у земли, гораздо более стабильны в стратосфере. С другой стороны, такие соединения, как закись азота, которые относительно инертны на земле, могут медленно подниматься в стратосферу, где они в конечном итоге вступают в реакцию с другими соединениями. Типичная (но очень изменчивая) продолжительность жизни NO x составляет несколько часов для нижней тропосферы и несколько дней для верхней тропосферы. В стратосфере и мезосфере типичная продолжительность жизни составляет от нескольких дней до нескольких недель.
Азотистая кислота могла образоваться в атмосфере в результате вероятной гетерогенной реакции.
- НЕТ+НЕТ2+ЧАС2О⟶2ЛОР2{\ displaystyle {\ ce {NO + NO2 + H2O -> 2 HNO2}}}
Однако затем он подвергается фотолизу , поэтому во многих химических моделях он рассматривается как источник радикалов ОН.
- ЛОР2+hv⟶ОЙ+НЕТ{\ displaystyle {\ ce {HNO2 + hv -> OH + NO}}}
Пятиокись азота может встречаться в атмосфере как промежуточное соединение. Возникает з. Б. из диоксида азота и триоксида азота.
- НЕТ2+НЕТ3↽—⇀N2О5{\ displaystyle {\ ce {NO2 + NO3 <=> N2O5}}}
Как ангидрид азотной кислоты, он реагирует с водой (паром) с образованием азотной кислоты, хотя скорость реакции в газовой фазе точно не известна.
- N2О5+ЧАС2О⟶2ЛОР3{\ displaystyle {\ ce {N2O5 + H2O -> 2 HNO3}}}
Предполагается, что реакция протекает преимущественно неоднородно на влажных аэрозолях. Также большое значение имеет образование азотной кислоты в атмосфере по реакции:
- ОЙ+НЕТ2+М.⟶ЛОР3+М.{\ displaystyle {\ ce {OH + NO2 + M -> HNO3 + M}}}
При 25 ° C реакция протекает примерно в десять раз быстрее, чем рекомбинация радикалов ОН с диоксидом серы. Но азотная кислота также может быть навсегда удалена из реакционного цикла, например Б. накоплением на аэрозольных частицах или новым образованием (конденсацией) таких частиц. Газообразная азотная кислота химически очень стабильна в тропосфере вблизи земли и удаляется из атмосферы путем сухого и влажного осаждения из-за ее хорошей растворимости в воде.
Триоксид азота, в свою очередь, является важной частью ночной чистой и загрязненной тропосферы. В течение дня соединение подвергается фотолизу:
- НЕТ3+hv⟶НЕТ+О2{\ displaystyle {\ ce {NO3 + hv -> NO + O2}}}
- НЕТ3+hv⟶НЕТ2+О{\ displaystyle {\ ce {NO3 + hv -> NO2 + O}}}
Кроме того, триоксид азота быстро реагирует с монооксидом азота с образованием диоксида азота:
- НЕТ3+НЕТ⟶2НЕТ2{\ displaystyle {\ ce {NO3 + NO -> 2NO2}}}
Таким образом, срок службы триоксида азота в течение дня составляет менее 10 с. Факторами, влияющими на эти реакции, являются концентрация озона, интенсивность света (солнце), время пребывания соединений в атмосфере, загрязнение воздуха (например, пыль, диоксид серы) и образование смога.
Признаки употребления
Первыми признаками могут оказаться ссадины на теле и синяки. Если человек вдохнет большое количество закиси, полностью погрузившись в наркоз, устоять ему на месте просто не удастся, он непременно упадет на землю и травмирует себя.
Баротравмы легких, обморожение ротовой полости, поскольку некоторые вдыхают его из баллончика, где давление газовой смеси составляет 40 атмосфер, что и приводит к таким последствиям. Вдыхание закиси азота на первых секундах не дает никакого эффекта, потом, спустя секунд 30 у человека происходит дефицит кислорода в головном мозге и он теряет сознание, в состоянии опьянения алкоголем, это особенно опасно. При передозировке веселящим газом, может сформироваться асфиксия – кислородное голодание и за этим последовать смерть.
Наркотическое опьянение веселящим газом длится примерно 30 минут, при повторном вдыхании оно может длится до нескольких часов. По силе напоминает алкогольное включающее в себя:
- существенное улучшение настроения;
- легкое головокружение и шум;
- приятную волну тепла по телу;
- расслабленность, смех, веселье;
- беспечность.
Именно в эти моменты у человека происходят галлюциногенные проявления и преимущественно приятные. Краски вокруг становятся яркими, звуки – четкими, прилив сил – зашкаливает.
https://youtube.com/watch?v=2s1Jg1k7_Xg
Оксид азота: свойства и все характеристики

В связи с тем, что в своих соединениях азот проявляет различные валентности, для этого элемента характерно несколько оксидов: оксид диазота, моно-, три-, ди- и пентаоксиды азота. Рассмотрим каждый из них более подробно.
Плохо растворяется в воде. При сильном охлаждении из раствора кристаллизуется кларат N2O×5,75H2O.
В твердом состоянии он полностью димеризован (N2O2), в жидком состоянии – частично (≈ 25% N2O2), в газе – в очень малой степени. Чрезвычайно термически устойчив. Плохо растворяется в воде.
При комнатной температуре на 90% разлагается на NOи NO2 и окрашивается в бурый цвет (NO2), не имеет температуры кипения (NO испаряется первым). В твердом состоянии – это белое или голубоватое вещество с ионным строением – нитрит нитрозила (NO+)(NO2—). В газе имеет молекулярное строение ON-NO2.
При температуре выше 135oС – это мономер, при комнатной температуре – красно-бурая смесь NO2 и его димера (тетраоксида диазота) N2O4. В жидком состоянии димер бесцветен, в твердом состоянии белый. Хорошо растворяется в холодной воде (насыщенный раствор – ярко-зеленый), полностью реагируя с ней.
При нагревании возгоняется и плавится, при комнатной температуре разлагается за 10 часов. В твердом состоянии имеет ионное строение (NO2+)(NO3—) – нитрат нитроила.
Таблица 1. Физические свойства оксидов азота.
| Молекулярная формула | N2O | NO | N2O3 | NO2 | N2O5 |
| Молярная масса, г/моль | 44 | 30 | 76 | 46 | 108 |
| Плотность, г/л | 1,9778 | 1,3402 | — | 2,0527 | — |
| Температура плавления, oС | -90,9 | -163,6 | -101 | -11,2 | 41 |
| Температура кипения, oС | -88,6 | -151,7 | 4,5 | 21,1 | — |
Получение оксида азота
В лабораторных условиях оксид диазота получают путем осторожного нагревания сухого нитрата аммония (1) или нагреванием смеси сульфаминовой и азотной (73%-ная) кислот (2):
NH4NO3 = N2O + 2H2O (1);
NH2SO2OH + HNO3 = N2O + H2SO4 + H2O (2).
Монооксид азота получают взаимодействием простых веществ азота и кислорода при высоких температурах (≈1300oС):
N2 + O2 = 2NO.
Кроме этого оксид азота (II) является одним из продуктов реакции растворения меди в разбавленной азотной кислоте:
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O.
При охлаждении смеси газов, состоящей из оксидов азота (II) и (IV) до -36oС образуется триоксид азота:
NO + NO2 = N2O3.
Данное соединение можно получить при действии 50%-ной азотной кислоты на оксид мышьяка (III) (3) или крахмал (4):
2HNO3 + As2O3 = NO2 + NO + 2HAsO3 (3);
HNO3 + (C6H10O5)n = 6nNO + 6nNO2 + 6nCO2 + 11nH2O (4).
Термическое разложение нитрата свинца (II) приводит к образованию диоксидазота:
2Pb(NO3)2 = 2PbO + 4NO2 + O2.
Это же соединение образуется при растворении меди в концентрированной азотной кислоте:
Cu + 4HNO3 = Cu(NO3)2 + 2NO2 + 2H2O.
Пентаоксид азота получают путем пропускания сухого хлора над сухим нитратом серебра (5), а также по реакции взаимодействия между оксидом азота (IV) и озоном (6):
2Cl2 + 4AgNO3 = 2N2O5 + 4AgCl + O2 (5);
2NO2 + O3 = N2O5 + O2 (6).
Химические свойства оксида азота
Оксид диазота малореакционноспособный, не реагирует с разбавленными кислотами, щелочами, гидратом аммиака, кислородом. При нагревании реагирует с колнцентрированной серной кислотой, водородом, металлами, аммиаком. Поддерживает горение углерода и фосфора. В ОВР может проявлять свойства как слабого окислителя, так и слабого восстановителя.
Монооксид азота не реагирует с водой, разбавленными кислотами, щелочами, гидратом аммиака. Мгновенно присоединяет кислород. При нагревании реагирует с галогенами и другими неметаллами, сильными окислителями и восстановителями. Вступает в реакции комплексообразования.
Триоксид азота проявляет кислотные свойства, реагирует с водой, щелочами, гидратом аммиака. Энергично реагирует с кислородом и озоном, окисляет металлы.
Пентаоксид азота проявляет кислотные свойства, реагирует с водой, щелочами, гидратом аммиака. Является очень сильным окислителем.
Применение оксида азота
Оксид диазота используют в пищевой промышленности (пропеллент при изготовлении взбитых сливок), медицине (для ингаляционного наркоза), а также в качестве основного компонента ракетного топлива.
Триоксид и диоксид азота применяются в неорганическом синтезе для получения азотной и серной кислот. Оксид азота (IV) также нашел применение в качестве одного из компонентов ракетного топлива и смесевых взрывчатых веществ.
Функция ЕСЛИ в Excel
Функция имеет следующий синтаксис.
ЕСЛИ(лог_выражение; значение_если_истина; )
лог_выражение – это проверяемое условие. Например, A2<100. Если значение в ячейке A2 действительно меньше 100, то в памяти эксель формируется ответ ИСТИНА и функция возвращает то, что указано в следующем поле. Если это не так, в памяти формируется ответ ЛОЖЬ и возвращается значение из последнего поля.
значение_если_истина – значение или формула, которое возвращается при наступлении указанного в первом параметре события.
значение_если_ложь – это альтернативное значение или формула, которая возвращается при невыполнении условия. Данное поле не обязательно заполнять. В этом случае при наступлении альтернативного события функция вернет значение ЛОЖЬ.
Очень простой пример. Нужно проверить, превышают ли продажи отдельных товаров 30 шт. или нет. Если превышают, то формула должна вернуть «Ок», в противном случае – «Удалить». Ниже показан расчет с результатом.
Продажи первого товара равны 75, т.е. условие о том, что оно больше 30, выполняется. Следовательно, функция возвращает то, что указано в следующем поле – «Ок». Продажи второго товара менее 30, поэтому условие (>30) не выполняется и возвращается альтернативное значение, указанное в третьем поле. В этом вся суть функции ЕСЛИ. Протягивая расчет вниз, получаем результат по каждому товару.
Однако это был демонстрационный пример. Чаще формулу Эксель ЕСЛИ используют для более сложных проверок. Допустим, есть средненедельные продажи товаров и их остатки на текущий момент. Закупщику нужно сделать прогноз остатков через 2 недели. Для этого нужно от текущих запасов отнять удвоенные средненедельные продажи.
Пока все логично, но смущают минусы. Разве бывают отрицательные остатки? Нет, конечно. Запасы не могут быть ниже нуля. Чтобы прогноз был корректным, нужно отрицательные значения заменить нулями. Здесь отлично поможет формула ЕСЛИ. Она будет проверять полученное по прогнозу значение и если оно окажется меньше нуля, то принудительно выдаст ответ 0, в противном случае — результат расчета, т.е. некоторое положительное число. В общем, та же логика, только вместо значений используем формулу в качестве условия.
В прогнозе запасов больше нет отрицательных значений, что в целом очень неплохо.
Сферы применения
Веселящий газ – это субстанция, которая на протяжении многих десятилетий используется в области анестезиологии. Применяют вещество при проведении операций, а также в стоматологии. Широкое распространение закись веселящего газа приобрела в гинекологии.
При соединении в оптимальных пропорциях с кислородом вещество оказывает на организм человека обезболивающий эффект, позволяет устранить нервное напряжение. Подобные свойства становятся полезными при лечении заболеваний хирургическим путем, в случае протезирования либо удаления зубов, в ходе родовой деятельности.
Первоначально, когда врачи до конца не понимали – что это веселящий газ, субстанция применялась без соединения с кислородом. Неразбавленное вещество предлагали вдыхать пациентам на протяжении нескольких минут, что нередко приводило задержкам дыхания и летальному исходу. Подобные случаи вызвали необходимость разработки специального агрегата, который создавал безопасную закись веселящего газа и кислорода. Правильное применение субстанции показало отсутствие вреда для самочувствия. Азот (веселящий газ) быстро выводился из организма и позволял человеку возвратиться к адекватному восприятию вещей.
В наши дни вещество находится в свободном доступе. Часто продавцы не отмечают, что веселящий газ – это довольно опасная субстанция, которую дозволено применять лишь в ограниченных дозах. Таким образом, сформировалось новое направление токсикомании.
Углекислый газ и мы: чем опасен СO2
Углекислый газ необходим человеческому организму так же, как кислород. Но так же, как с кислородом, переизбыток углекислого газа вредит нашему самочувствию.
Большая концентрация CO2 в воздухе приводит к интоксикации организма и вызывает состояние гиперкапнии. При гиперкапнии человек испытывает трудности с дыханием, тошноту, головную боль и может даже потерять сознание. Если содержание углекислого газа не снижается, то далее наступает черед гипоксии – кислородного голодания. Дело в том, что и углекислый газ, и кислород перемещаются по организму на одном и том же «транспорте» – гемоглобине. В норме они «путешествуют» вместе, прикрепляясь к разным местам молекулы гемоглобина. Однако повышенная концентрация углекислого газа в крови понижает способность кислорода связываться с гемоглобином. Количество кислорода в крови уменьшается и наступает гипоксия.
Такие нездоровые для организма последствия наступают при вдыхании воздуха с содержанием CO2 больше 5 000 ppm (таким может быть воздух в шахтах, например). Справедливости ради, в обычной жизни мы практически не сталкиваемся с таким воздухом. Однако и намного меньшая концентрация диоксида углерода отражается на здоровье не лучшим образом.
Согласно выводам некоторых исследований, уже 1 000 ppm CO2 вызывает у половины испытуемых утомление и головную боль. Духоту и дискомфорт многие люди начинают ощущать еще раньше. При дальнейшем повышении концентрации углекислого газа до 1 500 – 2 500 ppm критически снижается работоспособность, мозг «ленится» проявлять инициативу, обрабатывать информацию и принимать решения.
И если уровень 5 000 ppm почти невозможен в повседневной жизни, то 1 000 и даже 2 500 ppm легко могут быть частью реальности современного человека. Наш эксперимент в школе показал, что в редко проветриваемых школьных классах уровень CO2 значительную часть времени держится на отметке выше 1 500 ppm, а иногда подскакивает выше 2 000 ppm. Есть все основания предполагать, что во многих офисах и даже квартирах ситуация похожая.
Безопасным для самочувствия человека уровнем углекислого газа физиологи считают 800 ppm.
Еще одно исследование обнаружило связь между уровнем CO2 и окислительным стрессом: чем выше уровень диоксида углерода, тем больше мы страдаем от окислительного стресса, который разрушает клетки нашего организма.
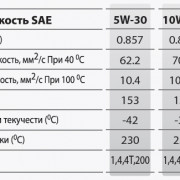
Физические свойства оксида азота (IV):
| Наименование параметра: | Значение: |
| Химическая формула | NO2 |
| Синонимы и названия иностранном языке | nitrogen dioxide (англ.)
nitrogen(IV) oxide (англ.) азота двуокись (рус.) азота диоксид (рус.) диазота тетраоксид (рус.) |
| Тип вещества | неорганическое |
| Внешний вид | красно-бурый газ или желтоватая жидкость |
| Цвет | красно-бурый, желтоватый |
| Вкус | —* |
| Запах | характерный острый запах |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | жидкость |
| Плотность (состояние вещества – жидкость, при 0 °C), кг/м
3 |
1491 |
| Плотность (состояние вещества – жидкость, при 0 °C), г/см
3 |
1,491 |
| Плотность (состояние вещества – газ), кг/м
3 |
2,0527 |
| Плотность (состояние вещества – газ), г/л | 2,0527 |
| Температура кипения, °C | 21,1 |
| Температура плавления, °C | -11,2 |
| Молярная масса, г/моль | 46,0055 |
Примечание:
* — нет данных.
Химические свойства
При взаимодействии с сильными окислителями 4-диоксид углерода проявляет окислительные свойства. Типичная реакция этого взаимодействия:
Так, при помощи угля диоксид углерода восстанавливается до своей двухвалентной модификации — угарного газа.
При нормальных условиях углекислый газ инертен. Но некоторые активные металлы могут в нем гореть, извлекая из соединения кислород и высвобождая газообразный углерод. Типичная реакция – горение магния:
2Mg + CO2 = 2MgO + C.
В процессе реакции образуется оксид магния и свободный углерод.
В химических соединениях СО2 часто проявляет свойства типичного кислотного оксида. Например, он реагирует с основаниями и основными оксидами. Результатом реакции становятся соли угольной кислоты.
Например, реакция соединения оксида натрия с углекислым газом может быть представлена так:
релиз
Веселящий газ в основном образуется как побочный продукт естественных процессов, например, в процессе бактериальной нитрификации , и выбрасывается в атмосферу. Как побочный продукт техногенных процессов, закись азота выделяется не только в процессе горения, но и в результате интенсивного . Растущее использование азотных удобрений в сельском хозяйстве в первую очередь является причиной антропогенных выбросов закиси азота . По сравнению с традиционным сельским хозяйством , органическое сельское хозяйство производит примерно на 40% меньше закиси азота на гектар.
| Источники закиси азота | глобальные выбросы [10 6 т / год] |
|---|---|
| природные источники | 6,6–12,2 |
| • Океаны / озера | 2,0-4,0 |
| • естественные почвы | 4.6-8.2 |
| антропогенные источники | 1,4-6,5 |
| • Сжигание биомассы | 0,2–2,4 |
| • Использование искусственных удобрений (почва и грунтовые воды) | 1,0–3,6 |
| все источники | 8,9-18,7 |
Другими возможными источниками являются фотохимические реакции в стратосфере и тропосфере и образование закиси азота катализаторами.
Азотные удобрения при определенных условиях превращаются в закись азота. Обычно N 2 O ферментативно расщепляется в почве. Медьсодержащий фермент монооксид-редуктаза диазота играет важную роль в продолжающемся биохимическом процессе , поскольку он превращает N 2 O в N 2 (→ денитрификация ). Однако этот фермент чувствителен к кислороду и часто дает сбой в цепочке реакций . Поэтому большие количества N 2 O выбрасываются с удобренных пахотных земель. При выращивании энергетических культур, таких как рапс, выделяется большее количество закиси азота из-за увеличения количества удобрений, особенно зимой. Выбросы N 2 O от выращивания рапса соответствуют выбросам от других полей. В результате с точки зрения выбросов N 2 O климатический баланс рапса более отрицательный, чем у бензина.
Концентрация веселящего газа в атмосфере Земли с первого года ( анализ керна льда , измерения на мысе Грим (Австралия), NOAA , март 2017 г.)
Более поздние исследования показали , что меры по снижению выбросов оксидов азота от процессов горения также приводят к значительному увеличению иногда в выбросах оксидов азота ( компромиссный ). Например, электростанции со сжиганием в циркулирующем псевдоожиженном слое , которые выделяют мало оксида азота из-за процесса, имеют очень высокие выбросы оксида азота. То же самое относится к автомобилям с регулируемым трехкомпонентным каталитическим нейтрализатором , влияние которого на глобальный бюджет N 2 O (по состоянию на 2017 год) все еще остается неопределенным.
В химической промышленности синтез адипиновой кислоты ( предшественника полиамида ) — это процесс, при котором выделяется веселящий газ.
При определенных условиях закись азота может также образовываться на твердых поверхностях при нормальных условиях . Впервые это было замечено в соленом озере в Антарктике.
В отличие от этих источников, в качестве стока, является фотохимическая деградация в стратосфере с примерно 20,5 · 10 6 т / год.
- N2О+ЧАСν⟶N2+О{\ displaystyle \ mathrm {N_ {2} O + h \ nu \ longrightarrow N_ {2} + O}}
- N2О+О⟶N2+О2{\ displaystyle \ mathrm {N_ {2} O + O \ longrightarrow N_ {2} + O_ {2}}}
- N2О+О⟶2 NО{\ displaystyle \ mathrm {N_ {2} O + O \ longrightarrow 2 \ NO}}
Количества, которые также распадаются за счет поглощения почвой и водными микроорганизмами, неизвестны.
Использует [ редактировать ]
НЕТ2используются в качестве промежуточного продукта в производстве азотной кислоты , в качестве нитрующего агента в производстве химических взрывчатых веществ , в качестве ингибитора полимеризации для акрилатов , в качестве отбеливающего агента муки ,. : 223 и в качестве стерилизующего средства при комнатной температуре. Он также используется в качестве окислителя в ракетном топливе , например, в красной дымящей азотной кислоте ; он использовался в ракетах «Титан» для запуска проекта «Близнецы» , в маневрирующих двигателях космического корабля «Шаттл» и в беспилотных космических аппаратах.отправляется на разные планеты.
Оксид углерода CO2(IV) — углекислый газ
Молекула углекислого газа имеет линейное строение (углерод имеет валентность 4, и степень окисления +4):
Атомы углерода и кислорода связаны ковалентными полярными связями, но сама молекула неполярна.
Углекислый газ (диоксид углерода) также, как и угарный газ, не имеет цвета, запаха, плохо растворим в воде, но, растворяется лучше, чем CO. При низких температурах углекислота переходит в жидкое, а затем в твердое состояние (сухой лед).
Углекислый газ реагирует со следующими веществами:
- при растворении в воде образует угольную кислоту:CO2+H2O = H2CO3
- с основными оксидами и основаниями CO2 взаимодействует, как кислотный оксид, образуя соли, которые называются карбонатами: Na2O+CO2 = Na2CO3
- при высоких температурах углекислый газ проявляется свойства окислителя — активные металлы могут гореть в среде углекислого газа, отнимая у него кислород: CO2+C = 2COCO2+2Mg = 2MgO+C
Получение и применение углекислого газа
- в промышленности — обжигом известняка:CaCO3 = CaO+CO2↑
- в лаборатории — действием кислоты на соли угольной кислоты:Na2CO3+2HCl = 2NaCl+H2O+CO2↑
- в природе углекислый газ выделяется при гниении и горении органических веществ:C+O2 = CO2↑
Углекислый газ нашел широкое применение в пищевой промышленности, в качестве основного компонента газированных напитков. Сухой лед применяется в качестве охладителя. Углекислотные огнетушители применяются при тушении похара, если температура горения не превышает 1000°C.
Если вам понравился сайт, будем благодарны за его популяризацию Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: Политика конфиденциальности Об авторе