Уроки по неорганической химии для подготовки к егэ
Содержание:
- Что такое Закись Азота
- Аммиак NH3
- Химические свойства
- Сферы применения
- Оксид азота NO2(IV)
- Получение[править | править код]
- Роль в живых организмах
- Химические свойства
- Что мы узнали?
- Тест по теме
- Токсичность и опасность
- Описание оксида пятивалентного азота
- Краткая характеристика оксида азота (IV):
- Литература[править | править код]
- Какие оксиды реагируют с водой?
- Проведение анализа на наличие диоксида азота
Что такое Закись Азота
Что такое? Оксид азота — бесцветный газ с характерным запахом, тяжелее воздуха (относительная плотность 1,527). Оксид азота применяется в медицине для наркоза. Химическая формула — N2О Содержание основного вещества( N2О) — не менее 97% Мощность производства — до 5,4 тыс. тонн в год Качество медицинской оксида азота соответствует требованиям Фармакопейной статьи ФС 42-2926-92. Свойства: При температуре 0 оС и давлении 40 ати закись азота сгущает-ся в бесцветную жидкость. Из 1 кг жидкой закиси азота образуется 500 л газа. Не воспламеняется, но поддерживает горение. Закись азота при вдыхании не вызывает раздражения дыхательных путей, с гемоглобином не связывается. После прекращения вдыхания через 10-15 минут полностью выделяется через дыхательные пути. Применяется в смеси с кислородом в качестве наркоза в хирурги-ческой практике, оперативной гинекологии, хирургической стоматологии, для обезболивания родов, для профилактики травматического шока в послеоперационный период, а также для купирования болевых приступов при острой коронарной недостаточности, инфаркте миокарда, остром панкреатите и других патало-гических состояниях, сопровождающихся болями. ТРЕБОВАНИЯ БЕЗОПАСНОСТИ Смеси с эфиром, циклопропаном , хлорэтилом в определенных концентрациях взрывоопасны. УПАКОВКА И ХРАНЕНИЕ Закись азота хранится в металлических баллонах вместимостью 10 л по 6,2 кг под давлением. Баллоны транспортируются в контейнерах и россыпью всеми видами транспорта в соответствии с правилами перевозки грузов, действующими на транспорте данного вида. ГАРАНТИЙНЫЙ СРОК ХРАНЕНИЯ — 5 ЛЕТ Зачем? Вы купили машину, которая, как вы думаете принадлежит к разряду быстрых. И внезапно замечаете, что есть машинки немного более резвые, чем ваша. Что делать? Продать старую и купить новую? Это решение для некоторых. Сделать тюнинг двигателя и ходовой? Это решение для других. Любой тюнинг — это соответствующее капиталовложение. Вы же потратили практически все деньги на покупку, регистрацию и прочую лабуду. И остались сзади. Что делать? Решение есть — поставить небольшую систему впрыска закиси азота. На обычную машину со стандартным компьютером. На автоматной HONDA RAFAGA с комплектом от ZEX на медицинском баллоне прибавка составила 1.7 сек на 400 метров. Соблюдая некоторые правила (включать не более 15 сек и затем охлаждать мотор), вы спокойно будете иметь запас по мощности 55-125 лошадиных сил. И в нужное время его применять. Если соберетесь продавать машину — проблем нет, система без следа демонтируется и легко ставится на другую. Как работает Закись азота под давлением в 1100 psi или 75 атм впрыскивается в камеры сгорания с помощью специальных форсунок. Вместе с закисью должно увеличится количество топлива впрыскиваемого в цилиндры. Это делается двумя способами. «Мокрый» способ — закись вместе с топливом впрыскивается в цилиндры через форсунки для закиси азота. Недостаток — необходимо контролировать давление в баллоне чтобы не обогатить смесью «Сухой» способ — закись впрыскивается через отдельную форсунку, а топливо через стандартные форсунки. Недостаток — ограниченная прибавочная мощность. Заправка Заправка — одна из самых главных проблем, с которой сталкиваются желающие поставить закись на свой автомобиль. Закись азота выпускается в России в баллонах по 6.5 кг вещества с давлением 45-50 атм. Это медицинские баллоны. Стоимость их низкая. Но есть проблемы с приобретением, так как до сих пор числится в разряде наркотиков. Первый и самый простой способ использовать эти баллоны. Для этого необходимо выточить бронзовую гайку под резьбу на русский баллон. В комплект ZEX входит контроллер, который позволяет ездить на том давлении, которое есть в баллоне, и иметь прибавку в мощности. В этом преимущество комплектов ZEX от конкурентов. При покупке обязательно надо проверять давление в баллонах, так как встречаются медицинские баллоны с очень низким давлением. Для этого очень хорошо иметь манометр в комплекте. Так же очень положительно влияет нагрев баллона до 30-35 градусов и расположение его в машине краном вниз. Второй способ — заправлять родной баллон, который идет в комплекте. Это можно делать с помощью соответствующего оборудования, например компрессора для заправки огнетушителей, и медицинских баллонов. Так же заправочную станцию можно приобрести от производителей систем впрыска закиси азота.
Аммиак NH3
Бинарное соединение , степень окисления азота равна – 3. Бесцветный газ с резким характерным запахом. Молекула имеет строение незавершенного тетраэдра [: N(H)3] (sp3-гибридизация). Наличие у азота в молекуле NH3 донорской пары электронов на sp3-гибридной орбитали обуславливает характерную реакцию присоединения катиона водорода, при этом образуется катион аммония NH4. Сжижается под избыточным давлением при комнатной температуре. В жидком состоянии ассоциирован за счет водородных связей. Термически неустойчив. Хорошо растворим в воде (более 700 л/1 л H2O при 20˚C); доля в насыщенном растворе равна 34% по массе и 99% по объему, pH= 11,8.
Весьма реакционноспособный, склонен к реакциям присоединения. Сгорает в кислороде, реагирует с кислотами. Проявляет восстановительные (за счет N-3) и окислительные (за счет H+1) свойства. Осушается только оксидом кальция.
Качественные реакции – образование белого «дыма» при контакте с газообразным HCl, почернение бумажки, смоченной раствором Hg2(NO3)2.
Промежуточный продукт при синтезе HNO3 и солей аммония. Применяется в производстве соды, азотных удобрений, красителей, взрывчатых веществ; жидкий аммиак – хладагент. Ядовит.
Уравнения важнейших реакций:
2NH3(г) N2 + 3H2NH3(г) + H2O NH3 * H2O (р) NH4++ OH—NH3(г) + HCl(г) NH4Cl(г) белый «дым»
4NH3 + 3O2 (воздух) = 2N2 + 6 H2O (сгорание)
4NH3 + 5O2 = 4NO+ 6 H2O (800˚C, кат. Pt/Rh)
2 NH3 + 3CuO = 3Cu + N2 + 3 H2O (500˚C)
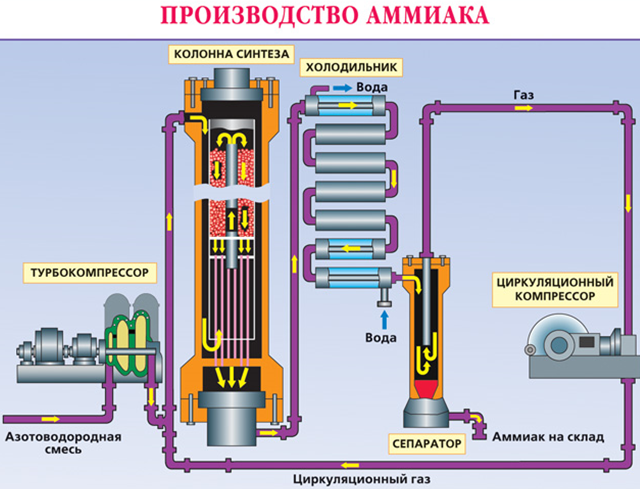
2 NH3 + 3Mg = Mg3N2 +3 H2 (600 ˚C )NH3(г) + CO2(г) + H2O = NH4HCO3 (комнатная температура, давление)Получение. В лаборатории – вытеснение аммиака из солей аммония при нагревании с натронной известью: Ca(OH)2 + 2NH4Cl = CaCl2+ 2H2O +NH3Или кипячение водного раствора аммиака с последующим осушением газа. В промышленности аммиак получают из азота с водородом. Выпускается промышленностью либо в сжиженном виде, либо в виде концентрированного водного раствора под техническим названием аммиачная вода.
 Гидрат аммиака NH3 *H2O. Межмолекулярное соединение. Белый, в кристаллической решетке – молекулы NH3 и H2O, связанные слабой водородной связью. Присутствует в водном растворе аммиака, слабое основание (продукты диссоциации – катион NH4 и анион OH). Катион аммония имеет правильно-тетраэдрическое строение (sp3-гибридизация). Термически неустойчив, полностью разлагается при кипячении раствора. Нейтрализуется сильными кислотами. Проявляет восстановительные свойства (за счет N-3) в концентрированном растворе. Вступает в реакцию ионного обмена и комплексообразования.
Гидрат аммиака NH3 *H2O. Межмолекулярное соединение. Белый, в кристаллической решетке – молекулы NH3 и H2O, связанные слабой водородной связью. Присутствует в водном растворе аммиака, слабое основание (продукты диссоциации – катион NH4 и анион OH). Катион аммония имеет правильно-тетраэдрическое строение (sp3-гибридизация). Термически неустойчив, полностью разлагается при кипячении раствора. Нейтрализуется сильными кислотами. Проявляет восстановительные свойства (за счет N-3) в концентрированном растворе. Вступает в реакцию ионного обмена и комплексообразования.
Химические свойства
Представляет собой типичный кислотный оксид. Вещество легко возгоняется и крайне неустойчиво. Разложение может происходить со взрывом, часто — без видимых побудительных причин:
- 2N2O5⟶4NO2↑+O2↑{\displaystyle {\ce {2N2O5->4NO2\uparrow +O2\uparrow }}}.
Бурно реагирует с водой с образованием азотной кислоты:
- N2O5+H2O⟶2HNO3{\displaystyle {\ce {N2O5 + H2O -> 2 HNO3}}}
Взаимодействует со щелочами с образованием соответствующих нитратов:
- N2O5+2NaOH⟶2NaNO3+H2O{\displaystyle {\ce {N2O5 + 2 NaOH -> 2 NaNO3 + H2O}}}.
Является сильным окислителем:
- N2O5+Na⟶NaNO3+NO2↑{\displaystyle {\ce {N2O5 + Na -> NaNO3 + NO2 ^}}},
- N2O5+I2⟶I2O5+N2↑{\displaystyle {\ce {N2O5 + I2 -> I2O5 + N2 ^}}}.
При взаимодействии с гемиоксидом хлора при охлаждении жидким воздухом образует нитрат хлора:
- Cl2O+N2O5⟶2ClNO3{\displaystyle {\ce {Cl2O + N2O5 -> 2ClNO3}}}.
Сферы применения
Веселящий газ – это субстанция, которая на протяжении многих десятилетий используется в области анестезиологии. Применяют вещество при проведении операций, а также в стоматологии. Широкое распространение закись веселящего газа приобрела в гинекологии.
При соединении в оптимальных пропорциях с кислородом вещество оказывает на организм человека обезболивающий эффект, позволяет устранить нервное напряжение. Подобные свойства становятся полезными при лечении заболеваний хирургическим путем, в случае протезирования либо удаления зубов, в ходе родовой деятельности.
Первоначально, когда врачи до конца не понимали – что это веселящий газ, субстанция применялась без соединения с кислородом. Неразбавленное вещество предлагали вдыхать пациентам на протяжении нескольких минут, что нередко приводило задержкам дыхания и летальному исходу. Подобные случаи вызвали необходимость разработки специального агрегата, который создавал безопасную закись веселящего газа и кислорода. Правильное применение субстанции показало отсутствие вреда для самочувствия. Азот (веселящий газ) быстро выводился из организма и позволял человеку возвратиться к адекватному восприятию вещей.
В наши дни вещество находится в свободном доступе. Часто продавцы не отмечают, что веселящий газ – это довольно опасная субстанция, которую дозволено применять лишь в ограниченных дозах. Таким образом, сформировалось новое направление токсикомании.
Оксид азота NO2(IV)
Строение молекулы:
Связи N-O располагаются под углом друг к другу, при этом они носят промежуточный «полуторный» характер, при этом имеется еще и один неспаренный электрон, как и у NO (см. выше).
При н.у. оксид азота NO2(IV) является ядовитым газом (хорошо растворимым в воде) бурого цвета, с характерным запахом.
Оксид азота NO2(IV) — смешанный оксид, ему соответствуют две кислоты: азотистая и азотная, поэтому, реакция взаимодействия с водой имеет следующий вид:2N+4O2+H2O = HN+3O2+HN+5O3
При нагревании до 50°C неустойчивая азотистая кислота не образуется:3NO2+H2O = 2HNO3+NO
На воздухе NO2 взаимодействует с водой с образованием только азотной кислоты:4N+4O2+O2+2H2O 4HN+5O3-2
Оксид азота NO2(IV) взаимодействует с растворами щелочей с образованием воды и двух солей — нитрата и нитрита:
2N+4O2+2NaOH = NaN+3O2+NaN+5O3+H2O
В избытке кислорода образуется только нитрат натрия:
4N+4O2+4NaOH+O2 = 4NaN+5O3-2+2H2O
При температуре ниже 22°C молекулы оксида азота NO2(IV) легко соединяются попарно (димеризуются), в результате чего образуется бесцветная жидкость, превращающаяся в кристаллы при дальнейшем охлаждении до температуры ниже -10,2°C.
В промышленных условиях оксид азота NO2(IV) получают путем окисления NO кислородом:2NO+O2=2NO2
Оксид азота NO2(IV) применяют в производстве азотной кислоты.
Получение[править | править код]
Путём дегидратации азотной кислоты HNO3{\displaystyle {\ce {HNO3}}} с помощью оксид фосфора(V) P2O5{\displaystyle {\ce {P2O5}}}:
- 2HNO3+P2O5⟶2HPO3+N2O5{\displaystyle {\ce {2 HNO3 + P2O5 -> 2 HPO3 + N2O5}}}.
Пропусканием сухого хлора над сухим нитратом серебра:
- 4AgNO3+2Cl2⟶4AgCl+2N2O5+O2↑{\displaystyle {\ce {4 AgNO3 + 2 Cl2 -> 4 AgCl + 2N2O5 + O2 ^}}},
(по другим данным, при этой реакции будет образовываться хлорид серебра и хлорнитрат).
Путём взаимодействия оксида азота(IV) с озоном:
- 2NO2+O3⟶N2O5+O2↑{\displaystyle {\ce {2 NO2 + O3 -> N2O5 + O2 ^}}}.
С 1983 года промышленное получение в основном осуществляется электролизом азотной кислоты в присутствии тетроксида диазота:
- 2HNO3⟶N2O5+H2O{\displaystyle {\ce {2 HNO3 -> N2O5 + H2O}}}.
Роль в живых организмах
Роль оксида азота (II) как сигнальной молекулы в живых организмах была открыта в 1980-х годах, а в 1998 Роберт Ферчготт, Луис Игнарро и Ферид Мурад получили Нобелевскую премию по физиологии или медицине за выяснение его функций в сердечно-сосудистой системе. Монооксид азота является паракринным фактором благодаря своей способности быстро диффундировать через мембраны клеток, однако из-за высокой реакционность расстояние такой диффузии ограничена 1 мм а время полжизни молекул NO составляет 5-10 секунд. Азот мооноксид выполняет сигнальную функцию как у животных, так и у растений, даже некоторые бактерии могут чувствовать очень небольшие его концентрации и двигаться в сторону от источника этого соединения.
У млекопитающих NO задействован в ряде физиологических процессов, таких как регуляция артериального давления, передача нервных импульсов, свертывания крови и иммунный ответ. Синтез оксида азота (II) осуществляется путем деаминирование аминокислоты аргинина и обеспечивается ферментом NO-синтазы (NOS), что у млекопитающих трех изоформы: нейрональная (nNOS), индуцибельной (iNOS) и эндотелиальной (eNOS). nNOS и eNOS экспрессируются в соответствующих типах клеток конститутивно и резко увеличивают свою активность в ответ на рост концентрации Ca 2+. Зато активация iNOS осуществляется на уровне транскрипции под влиянием эндотоксинов или цитокинов воспаления, в частности в таких клетках как макрофаги и нейтрофилы, и не зависит от цитоплазматического уровня кальция.
Одной из мишеней монооксида азота в клетках млекопитающих, в том числе и гладких мышцах, является фермент гуанилатциклазы, в активном центре которого он присоединяется к атому железа и таким образом увеличивает энзиматическую активность. Циклический ГМФ, что является продуктом гуанилатциклазы, является вторичным посредником и запускает в клетке каскад реакций, обеспечивающих физиологическую ответ, в случае гладких мышц — их расслабление.
NO может действовать также и цГМФ-независимым путем, например изменять активность белков путем ковалентной нитрозилювання тиольных групп (-SH) специфических остатков цистеина в их составе.
Защитная функция монооксида азота
У растений NO участвует в защитных реакциях во время повреждений и инфекций. Также монооксид азота играет роль в функционировании иммунной системы животных. Активированные макрофаги и нейрофилов (а также клетки эндотелия) производят его в больших количествах во время воспалительных процессов. Вместе с NO они выделяют супероксид-он (O-2), эти два соединения соединяясь образуют очень токсичен пероксинитрит (OONO -) нужен для того, чтобы убить поглощены бактерии.
Медицинские препараты, влияющие на сигналювання NO
Из препаратов, влияющих на сигнальный путь монооксида азота, первым начал использоваться еще в XIX веке нитроглицерин для борьбы со стенокардией. Это соединение медленно расщепляется в организме и действует как источник NO длительное время. NO в свою очередь обеспечивает расширение сосудов и уменьшения нагрузки на сердце. Такое действие нитроглицерина была открыта благодаря наблюдению, что больные стенокардией работники фабрик, на которых изготавливали это соединение, сильнее страдали от боли на выходных
Врачи настолько часто слышали такие сообщения пациентов, обратили внимание на терапевтический эффект нитроглицерина. С тех пор было разработано много других нитровазодиляторив
Сам NO не имеет терапевтического действия при стенокрадии, через очень небольшое время полжизни, однако его иногда используют в вдыхаемой форме для облегчения легочной гипертензии.
Существуют также препараты, имеющие другие мишени в сигнальном пути NO. Например, силденафил подавляет деятельность фосфодиэстеразы, которая расщепляет цГМФ, таким образом продолжая продолжительность действия сигнала. Это соединение была впервые предложена для лечения стенокрадии, однако выяснилось, что она наиболее эффективно влияет на изоформу цГМФ-фосфодиэстеразы, експресуетсья в сосудах пениса, и вызывает их расширение и, соответственно, эрекцию. Поэтому силденафил (под названием Виагра) стал использоваться для лечения эректильной дисфункции.
Химические свойства
Основные реакции оксидов азота с простыми и сложными веществами приведены в таблице.
|
Оксиды |
Реакции |
Уравнения |
|
N2O |
При нагревании разлагается. Окисляет неметаллы. Проявляет свойства восстановителя с сильными окислителями. Реагирует с аммиаком и его производными. Не образует солей. Не реагирует с водой, щелочами, кислотами |
– 2N2O → 2N2 + O2; – 2N2O + C → 2N2 + CO2; – 5N2O + 8KMnO4 + 7H2SO4 → 5Mn(NO3)2 + 3MnSO4 + 4K2SO4 + 7H2O; – 2NH3 + N2O → NH4N3 + H2O; – 2NaNH2 + N2O → NaN3 + NaOH + NH3 |
|
NO |
Окисляется до диоксида азота на воздухе при нормальных условиях. Взаимодействует с галогенами. В присутствии сильного восстановителя проявляет окислительные свойства. Не образует соли, плохо растворим в воде |
– 2NO + O2 → 2NO2; – 2NO + Cl2 → 2NOCl; – 2SO2 + 2NO → 2SO3 + N2 |
|
N2O3 |
Разлагается при нагревании. Реагирует с водой с образованием азотистой кислоты. Растворим в щелочах |
– N2O3 → NO + NO2; – N2O3 + H2O → 2HNO2; – N2O3 + 2KOH → 2KNO2 + H2O |
|
NO2 |
Реагирует с неметаллами, металлами, галогенами, водой. Окисляет оксиды серы. Растворяется в щелочах |
– 10NO2 + 8P → 4P2O5 + 5N2; – 4NO2 + Zn → Zn(NO3)2 + 2NO; – 2NO2 + 2Cl2 → NOCl + NO2Cl + Cl2O; – 2NO2 + H2O → HNO3 + HNO2; – NO2 + SO2 → SO3 + NO; – 2NO2 + 2KOH → KNO3 + KNO2 + H2O |
|
N2O5 |
Быстро разлагается с взрывом. Растворяется в воде, щелочах |
– 2N2O5 → 4NO2 + O2; – N2O5 + H2O 2HNO3; – N2O5 + 2NaOH → 2NaNO3 + H2O |
Рис. 3. Пентаоксид диазота или оксид азота (V).
Оксиды используются для получения азотной кислоты. N2O используется в качестве наркоза.
Что мы узнали?
Из темы урока узнали, что азот может образовывать пять стабильных оксидов, проявляя переменную валентность I, II, III, IV, V. Только один оксид (NO) можно получить непосредственным взаимодействием азота и кислорода при нагревании или под воздействием электричества. Остальные оксиды выделяются из солей аммония и азотной кислоты. Большинство оксидов – токсичные газы, способные сжижаться. Оксиды реагируют с металлами, неметаллами, щелочами, оксидами.
Тест по теме
-
Вопрос 1 из 10
Начать тест(новая вкладка)
Токсичность и опасность
Воздух рабочей зоны
| ПДК максимальная разовая, мг/м3 | 2 |
| Класс опасности | 3 |
| Особенности токсического действия вещества на организм | остронаправленный механизм действия, требующий автоматического контроля за содержанием вещества в воздухе (О) |
Атмосферный воздух населённых мест
| ПДК максимальная разовая, мг/м3 | 0,4 |
| ПДК среднесуточная, мг/м3 | 0,06 |
| Класс опасности | 3 |
| Лимитирующий показатель вредности | Рефлекторно-резорбтивный |
Аварийные гигиенические регламенты и референтные уровни
| Аварийные пределы воздействия
отравляющих веществ в воздухе (АПВ, мг/м³) |
|
||||||
| Референтные концентрации для
хронического ингаляционного |
0,06 | ||||||
| Поражаемые органы и системы | органы дыхания, кровь (образование MetHb ) | ||||||
| Субъективная реакция дискомфорта (мг/м³) |
0,5 |
Опасность при утечке
Вещество может всасываться в организм при вдыхании. При утечке содержимого очень быстро достигается опасная концентрация этого газа в воздухе. Вещество раздражает глаза и дыхательные пути. Вдыхание этого вещества может вызвать отек легких. Вещество может оказывать действие на кровь , приводя к образованию метгемоглобина. Воздействие может вызвать смерть. Эффекты могут быть отсроченными. Вещество является сильным окислителем и реагирует с горючими материалами и восстановителями. При контакте с воздухом выделяет диоксид азота.
Острая токсичность
| Токсичность для животных |
|
||||
|
Токсичность для человека |
| Тип дозы | Способ измерения | Механизм воздействия | Состояние человека | Значение |
|---|---|---|---|---|
| Мгновенно-опасная для жизни или здоровья концентрация (IDLH) | в целом на организм | ингаляционно | в состоянии покоя | 122,7 мг/м3 |
| Пороговая токсодоза (PCt50, мг.мин/л) | 1,5 |
| Смертельная токсодоза (LCt50, мг.мин/л) | 18 |
Описание оксида пятивалентного азота
Его также называют диазотным пентаоксидом, нитратом нитрония, нитриловым нитратом или азотным ангидридом.
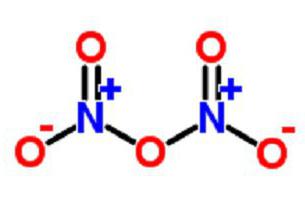
Существует в форме бесцветных кристаллов, которые обладают летучестью и неустойчивостью. Их стабильность наблюдается при низкой температуре. Такую структуру образуют нитрат- и нитрит-ионы.
В газообразном виде вещество имеет форму ангидрида NO2−O−NO2.
Оксид азота пятивалентный обладает свойствами кислотными. Он легко разлагается с выделением кислорода.
Вещество реагирует с водой, в результате получается азотная кислота.
Щелочи растворяют ангидрид с выделением солей нитратов.
Краткая характеристика оксида азота (IV):
Оксид азота (IV) – неорганическое вещество, ядовитый газ, красно-бурого цвета, с характерным острым запахом или желтоватая жидкость.
Оксид азота (IV) содержит один атом азота и два атома кислорода.
Химическая формула оксида азота (IV) NO2.
В обычном состоянии NO2 существует в равновесии со своим димером N2O4. Склонность к его образованию объясняется наличием в молекуле NO2 неспаренного электрона.
При температуре 140 °C оксид азота (IV) состоит только из молекул NO2, но очень тёмного, почти чёрного цвета.
В точке кипения NO2 – +21,1 °C представляет собой желтоватую жидкость, содержащую около 0,1 % NO2.
При температуре ниже +21°С – это бесцветная жидкость (или желтоватая из-за примеси мономера).
При температуре ниже −12 °C белые кристаллы состоят только из молекул N2O4.
Кислотный оксид.
Оксид азота (IV) высокотоксичен. Даже в небольших концентрациях он раздражает дыхательные пути, в больших концентрациях вызывает отёк лёгких.
Литература[править | править код]
Оксиды
| H2O | ||||||||||||||||
| Li2OLiCoO2Li3PaO4Li5PuO6Ba2LiNpO6LiAlO2Li3NpO4Li2NpO4Li5NpO6LiNbO3 | BeO | B2O3 | С3О2C12O9COC12O12C4O6CO2 | N2ONON2O3N4O6NO2N2O4N2O5 | O | F | ||||||||||
| Na2ONaPaO3NaAlO2Na2PtO3 | MgO | AlOAl2O3NaAlO2LiAlO2AlO(OH) | SiOSiO2 | P4OP4O2P2O3P4O8P2O5 | S2OSOSO2SO3 | Cl2OClO2Cl2O6Cl2O7 | ||||||||||
| K2OK2PtO3KPaO3 | CaOCa3OSiO4CaTiO3 | Sc2O3 | TiOTi2O3TiO2TiOSO4CaTiO3BaTiO3 | VOV2O3V3O5VO2V2O5 | FeCr2O4CrOCr2O3CrO2CrO3MgCr2O4 | MnOMn3O4Mn2O3MnO(OH)Mn5O8MnO2MnO3Mn2O7 | FeCr2O4FeOFe3O4Fe2O3 | CoFe2O4CoOCo3O4CoO(OH)Co2O3CoO2 | NiONiFe2O4Ni3O4NiO(OH)Ni2O3 | Cu2OCuOCuFe2O4Cu2O3CuO2 | ZnO | Ga2OGa2O3 | GeOGeO2 | As2O3As2O4As2O5 | SeOCl2SeOBr2SeO2Se2O5SeO3 | Br2OBr2O3BrO2 |
| Rb2ORbPaO3Rb4O6 | SrO | Y2O3YOFYOCl | ZrO(OH)2ZrO2ZrOSZr2О3Сl2 | NbONb2O3NbO2Nb2O5Nb2O3(SO4)2LiNbO3 | Mo2O3Mo4O11MoO2Mo2O5MoO3 | TcO2Tc2O7 | Ru2O3RuO2Ru2O5RuO4 | RhORh2O3RhO2 | PdOPd2O3PdO2 | Ag2OAg2O2 | Cd2OCdO | In2OInOIn2O3 | SnOSnO2 | Sb2O3Sb2O4Hg2Sb2O7Sb2O5 | TeO2TeO3 | I2O4I4O9I2O5 |
| Cs2OCs2ReCl5O | BaOBaPaO3BaTiO3BaPtO3 | HfO(OH)2HfO2 | Ta2OTaOTaO2Ta2O5 | WO2Br2WO2WO2Cl2WOBr4WOF4WOCl4WO3 | Re2OReORe2O3ReO2Re2O5ReO3Re2O7 | OsOOs2O3OsO2OsO4 | Ir2O3IrO2 | PtOPt3O4Pt2O3PtO2K2PtO3Na2PtO3PtO3 | Au2OAuOAu2O3 | Hg2OHgO(Hg3O2)SO4Hg2O(CN)2Hg2Sb2O7Hg3O2Cl2Hg5O4Cl2 | Tl2OTl2O3 | Pb2OPbOPb3O4Pb2O3PbO2 | BiOBi2O3Bi2O4Bi2O5 | PoOPoO2PoO3 | At | |
| Fr | Ra | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | |
| ↓ | ||||||||||||||||
| La2O2SLa2O3 | Ce2O3CeO2 | PrOPr2O2SPr2O3Pr6O11PrO2 | NdONd2O2SNd2O3NdHO | Pm2O3 | SmOSm2O3 | EuOEu3O4Eu2O3EuO(OH)Eu2O2S | Gd2O3 | Tb | Dy2O3 | Ho2O3Ho2O2S | Er2O3 | Tm2O3 | YbOYb2O3 | Lu2O2SLu2O3LuO(OH) | ||
| Ac2O3 | UO2UO3U3O8 | PaOPaO2Pa2O5PaOS | ThO2 | NpONpO2Np2O5Np3O8NpO3 | PuOPu2O3PuO2PuO3PuO2F2 | AmO2 | Cm2O3CmO2 | Bk2O3 | Cf2O3 | Es | Fm | Md | No | Lr |
Какие оксиды реагируют с водой?
Из всех оксидов с водой реагируют только:
1) все активные основные оксиды (оксиды ЩМ и ЩЗМ);
2) все кислотные оксиды, кроме диоксида кремния (SiO2);
т.е. из вышесказанного следует, что с водой точно не реагируют:
1) все малоактивные основные оксиды;
2) все амфотерные оксиды;
3) несолеобразующие оксиды (NO, N2O, CO, SiO).
Примечание:
Оксид магния медленно реагирует с водой при кипячении. Без сильного нагревания реакция MgO с H2O не протекает.
Способность определить то, какие оксиды могут реагировать с водой даже без умения писать соответствующие уравнения реакций, уже позволяет получить баллы за некоторые вопросы тестовой части ЕГЭ.
Теперь давайте разберемся, как же все-таки те или иные оксиды реагируют с водой, т.е. научимся писать соответствующие уравнения реакций.
Активные основные оксиды, реагируя с водой, образуют соответствующие им гидроксиды. Напомним, что соответствующим оксиду металла является такой гидроксид, который содержит металл в той же степени окисления, что и оксид. Так, например, при реакции с водой активных основных оксидов K+12O и Ba+2O образуются соответствующие им гидроксиды K+1OH и Ba+2(OH)2:
K2O + H2O = 2KOH – гидроксид калия
BaO + H2O = Ba(OH)2 – гидроксид бария
Все гидроксиды, соответствующие активным основным оксидам (оксидам ЩМ и ЩЗМ), относятся к щелочам. Щелочами называют все хорошо растворимые в воде гидроксиды металлов, а также малорастворимый гидроксид кальция Ca(OH)2 (как исключение).
Взаимодействие кислотных оксидов с водой так же, как и реакция активных основных оксидов с водой, приводит к образованию соответствующих гидроксидов. Только в случае кислотных оксидов им соответствуют не основные, а кислотные гидроксиды, чаще называемые кислородсодержащими кислотами. Напомним, что соответствующей кислотному оксиду является такая кислородсодержащая кислота, которая содержит кислотообразующий элемент в той же степени окисления, что и в оксиде.
Таким образом, если мы, например, хотим записать уравнение взаимодействия кислотного оксида SO3 с водой, прежде всего мы должны вспомнить основные, изучаемые в рамках школьной программы, серосодержащие кислоты. Таковыми являются сероводородная H2S, сернистая H2SO3 и серная H2SO4 кислоты. Cероводородная кислота H2S, как легко заметить, не является кислородсодержащей, поэтому ее образование при взаимодействии SO3 с водой можно сразу исключить. Из кислот H2SO3 и H2SO4 серу в степени окисления +6, как в оксиде SO3, содержит только серная кислота H2SO4. Поэтому именно она и будет образовываться в реакции SO3 с водой:
H2O + SO3 = H2SO4
Аналогично оксид N2O5, содержащий азот в степени окисления +5, реагируя с водой, образует азотную кислоту HNO3, но ни в коем случае не азотистую HNO2, поскольку в азотной кислоте степень окисления азота, как и в N2O5, равна +5, а в азотистой — +3:
N+52O5 + H2O = 2HN+5O3
Исключение:
Оксид азота (IV) (NO2) является оксидом неметалла в степени окисления +4, т.е. в соответствии с алгоритмом, описанным в таблице в самом начале данной главы, его нужно отнести к кислотным оксидам. Однако не существует такой кислоты, которая содержала бы азот в степени окисления +4.
В случае оксида NO2 принято считать, что ему соответствуют сразу две кислоты, поскольку его взаимодействие с водой приводит к одновременному образованию двух кислот:
2NO2 + H2O = HNO2 + HNO3
Проведение анализа на наличие диоксида азота
Для выявления диоксида азота в воздухе, а также определения его концентрации может использоваться несколько методов. Их эффективность зависит от конкретной ситуации, а выбор осуществляется профильными специалистами. Среди самых распространенных методов можно назвать высокоэффективную газовую хроматографию и гравиметрию.
- Газовая хроматография представляет собой физико-химический метод, который реализуется посредством разделения компонентов тестируемой смеси между двумя фазами, движущимися относительно друг друга. В роли подвижной фазы используется сам газ, в то время как неподвижной может быть жидкость или сорбент, находящийся в твердом состоянии.
- Гравиметрия – это количественный анализ, который основан на определении массы выявляемого вещества. В связи с этим при реализации метода применяется закон сохранения массы. К преимуществам гравиметрии можно отнести низкий процент погрешности, не превышающий 0,2%, а также возможность отказа от предварительной градуировки измерительных приборов. Однако такой метод более трудоемкий и затратный по времени.